Klinikk
Screening forebygger forekomst og død av kolorektal kreft
Øyvind Holme. Medisinsk avdeling, Sørlandet Sykehus Kristiansand
Gruppe for klinisk effektforskning, Institutt for helse og samfunn, Universitetet i Oslo

Øyvind Holme
Det er kun et spørsmål om tid før screening for kolorektal kreft innføres i Norge.
Men hvilken test bør vi velge? Er vi godt nok forberedt?
Bakgrunn
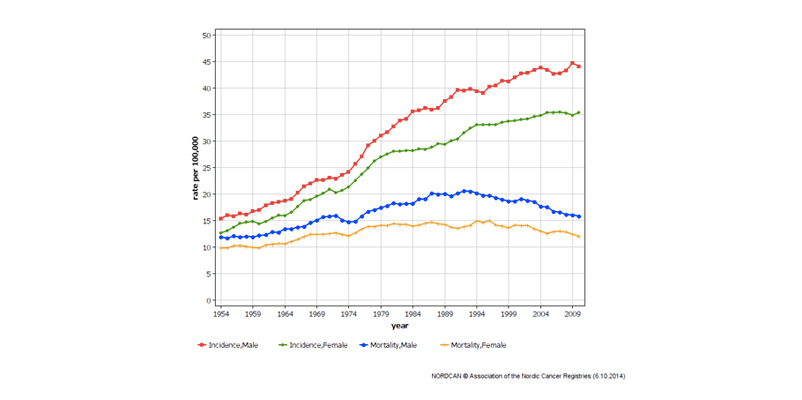
Kolorektal kreft (KRK) er den nest hyppigste kreftformen i Norge, og insidensen er økende (Figur 1). Hvert år får mer enn 3600 nordmenn diagnosen, og om lag 1600 dør.1 KRK utvikles fra polypper, de fleste adenomer, i kolon og rektum gjennom en årelang prosess, kalt adenom-carcinom sekvensen. Det er anslått at utvikling fra adenom til invasiv kreft kan ta så mye som 10-15 år.2 Adenomer gir som regel ingen symptomer. Symptomene på KRK er ofte vage og uspesifikke, og mange pasienter har derfor avansert sykdom når de blir diagnostisert. Overlevelse ved KRK er nært knyttet til stadium ved diagnosetidspunkt. Mens Dukes A KRK har en 5-års overlevelse på mer enn 95%, har pasienter med Dukes D under 10% 5-års overlevelse.3

Figur 1: Tidstrend for KRK insidens og mortalitet i Norge for menn og kvinner. Ratene er aldersstandardiserte.
Forebygging vs tidlig deteksjon
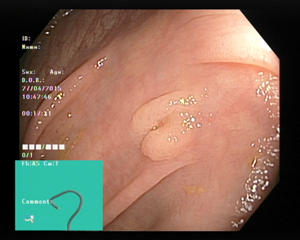
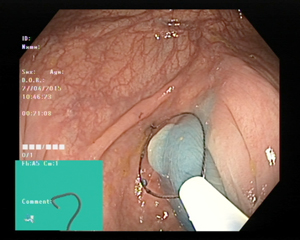
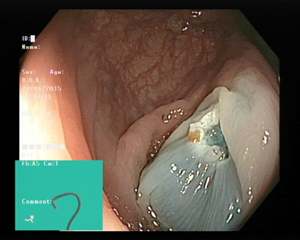
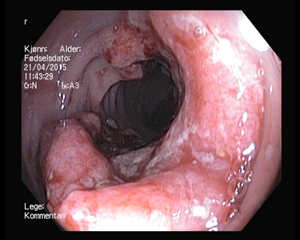
Screening er undersøkelse av personer som ikke har symptomer på den aktuelle sykdommen. Tidsvinduet for screening for KRK er derfor fra det tidspunktet adenomet oppstår til kreftsykdommen gir symptomer. Screening for KRK er innført i mange land og har prinsipielt to virkningsmekanismer: Forebygging og tidlig deteksjon (Figur 2). Ved forebygging ønsker man å finne og fjerne adenomet, som er forstadiet til KRK. Ved endoskopisk polyppektomi (Figur 3) vil man således kunne avbryte adenom-carcinom sekvensen (Figur 4). Insidensen av KRK vil da reduseres, og som en følge av dette vil det også bli en nedgang i mortalitet av KRK. Eksempler på screening metoder som kan redusere forekomst av KRK er koloskopi og sigmoideoskopi. Cytologisk undersøkelse av livmorhalsen er en annen screening metode som reduserer forekomst av sykdommen det screenes for.
Tidlig deteksjon går ut på å finne kreftsykdommen i et så tidlig stadium som mulig, for dermed å kunne tilby kurativ behandling. En screening-test som bare er i stand til å påvise tidlig sykdom, og ikke forstadier, vil derfor bare kunne reduserer mortalitet, og
ikke insidens. Mammografi og PSA-screening for prostatakreft vil ikke redusere insidens av sykdommen det screenes for. Koloskopi og sigmoideoskopi vil kunne redusere KRK mortalitet gjennom tidlig deteksjon (i tillegg til forebygging). Undersøkelse på okkult blod i avføringen (FOBT) har vært brukt som screening-test for KRK i mange år. FOBT er en tidlig deteksjonstest som ikke reduserer insidens av KRK, da adenomer sjelden blør og dermed ikke detekteres av testen. Det er gjort fire store randomiserte kontrollerte studier av FOBT der testen er repetert med 1-2 årsintervaller sammenlignet med en kontrollgruppe som ikke ble tilbudt noen screening. Meta-analyse av disse studiene viste at mortaliteten ble redusert med 14% i screening gruppen sammenlignet med kontrollgruppen.4 Meta-analysen bekreftet at insidens ikke ble redusert ved FOBT screening. Det skal nevnes at det i disse studiene ble brukt guaiac-baserte avføringstester med lav sensitivitet for KRK. Nyere tester basert på immunhistokjemisk påvisning av humant blod (faecal immunochemical testing – FIT) har vist bedre sensitivitet for KRK med bare marginalt lavere spesifistet.5 Disse testene har imidlertid aldri blitt evaluert i prospektive studier med mortalitet og forekomst av KRK som endepunkt. FIT har også høyere sensitivitet for adenomer enn guaiac-baserte FOBT. Om FIT dermed også kan redusere insidens av KRK er mulig, men foreløpig foreligger ingen resultater fra prospektive studier på dette.
Norsk forskning i førersetet
Norske forskere, med Geir Hoff (Kreftregisteret og Sykehuset Telemark) i spissen, har vært toneangivende i forskning på screening for KRK. I 1983 startet den såkalte Telemark Polyp Study (TPS). 799 friske menn og kvinner i alderen 50-59 år bosatt i Telemark fylke ble randomisert til å bli invitert til screening med sigmoideoskopi (endoskopisk undersøkelse av rektum og sigmoideum) eller ingen screening, og 81% møtte. Etter 13 års oppfølging var insidens av KRK redusert med 80%; relativ risiko 0,2 (95% Konfidens Intervall [KI] 0,03-0,95).6 Dette var den første prospektive studien i verden som viste at endoskopisk screening med polyppektomi kan redusere insidens av KRK.
NORCCAP-studien
Selv om TPS viste signifikant redusert insidens av KRK, var studien liten. I løpet av 90-tallet ble det initiert 4 store randomiserte kontrollerte studier i Europa og USA der screening med sigmoideoskopi ble sammenlignet med ingen screening, deriblant den norske Norwegian Colorectal Cancer Prevention Trial (NORCCAP).7-10 Lang-tids oppfølging av denne studien ble nylig publisert i JAMA9: I 1998 og i 2000 ble alle innbyggere i Telemark fylke og Oslo kommune i alderen 50-64 år identifisert gjennom Folkeregisteret. Det eneste eksklusjonkriteriet var tidligere diagnostisert KRK. 20 572 personer ble randomisert til å bli invitert til screening med sigmoideoskopi i perioden 1999-2001, og 63% møtte (halvparten ble også bedt om å avgi en avføringsprøve til FIT). 78 220 personer utgjorde kontrollgruppen. Personene i kontrollgruppen fikk aldri noe tilbud om screening. Oppfølgingen var registerbasert, via Kreftregisteret og Dødsårsaksregisteret. Etter median 10,9 år var insidens av KRK redusert med 20%; hazard ratio [HR] 0,80 (95% KI 0,70-0,92) og mortalitet med 27%; HR 0,73 (95% KI 0,56-0,94). Våre resultatene var forenlig med funnene i de andre studiene der KRK insidens var redusert med 18-23% og KRK mortalitet med 22-31%. I motsetning til de andre studiene som inkluderte pasienter fra 55 års alder, var også aldersgruppen 50-54 år inkludert i NORCCAP. Vi fant at screening reduserte insidens av KRK like mye for de yngste deltagerne i studien (50-54 åringene; HR 0,68, 95% KI 0,49-0,95) som for de eldste (55-64 åringene; HR 0,83, 95% KI 0,72-0,97). Dette indikerer at personer helt ned til 50 års alder har effekt av sigmoideoskopiscreening.
Norsk screening-pilotprosjekt
I 2012 ble det startet et pilot-prosjekt på screening for KRK i Norge, og prosjektet er organisert som en randomisert kontrollert studie.11 140 000 innbyggere i alderen 50-74 år i Østfold, Buskerud og Akershus er planlagt randomisert over en seks-årsperiode til enten en-gangs screening med sigmoideoskopi eller FIT annethvert år i 10 år. Endepunkt er insidens og mortalitet av KRK etter 10 år. Det norske pilotprosjektet har blitt kritisert for ikke å inkludere koloskopi som primær screening-metode. Koloskopi regnes som gullstandard innen KRK screening og har potensiale til å oppdage og fjerne polypper også i den proksimale delen av tykktarmen. Hvilken test som bør foretrekkes (FIT, sigmoideoskopi eller koloskopi) er imidlertid ikke åpenbart, og det finnes entusiaster i alle leire. Kostnad-nytte analyser viser at alle de tre nevnte metodene er kostnadseffektive, men ingen av de tre metodene har i disse analysene vist seg å være definitivt mer kostnadseffektiv enn de andre.12 Det foreligger forøvrig ingen resultater fra prospektive studier med koloskopi som primær screeningmetode, men 4 studier er pågående. En av disse en den norsk-initierte NordICC-studien (Nordic-European Initiative on Colorectal Cancer screening) der om lag 60 000 personer i Norge, Polen og Nederland ble randomisert til enten screening med koloskopi eller til en kontrollgruppe som ikke mottok noen invitasjon til screening.13 Inklusjon av pasienter til denne studien er nylig avsluttet, og resultatene er derfor ikke klare før om 10-15 år. Observasjonsstudier anslår at koloskopi reduserer KRK insidens og mortalitet fra KRK med 70%, noe som sannsynligvis er et overestimat.14 Tabell 1 gir en oversikt over screening metoder for KRK.
Fremtidig screening i Norge
Norge er et av få vestlige land uten noe tilbud til befolkningen om screening for KRK. Etter at resultatene fra NORCCAP-studien ble publisert i JAMA i høst (2014), uttalte helseministeren til Aftenposten 13. august at han ønsker å avvente resultater fra flere pilot-prosjekter før han eventuelt bestemmer seg for hva slags screening Norges befolkning skal tilbys. Dette kan synes som en passiv og uforståelig holdning. KRK er den nest hyppigste kreftformen i Norge. Insidensen i vårt land er økende, og øker mer enn i de andre nordiske landene. Vi har gode resultater fra randomiserte prospektive studier for at screening både forebygger KRK og reduserer dødeligheten av sykdommen. Vi har til og med data fra 4 norske studier om oppmøte til screening for KRK ved både koloskopi, sigmoideoskopi og FIT. Det finnes ikke et land i verden med bedre forskningsdata fra egen befolkning enn Norge, men likevel vil jeg fraråde innføring av screening for KRK i Norge nå.
Vi er dårlig forberedt
Koloskopi er en begrenset ressurs i Norge som i mange andre land. I følge data fra Norsk Pasient Register utføres om lag 70 000 koloskopier årlig i Norge (både polikliniske og på inneliggende pasienter). Uansett hvilken screeningmetode for KRK man måtte velge, vil innføring av screening føre til et stort behov for koloskopier. Og signifikante funn (adenomer og andre store polypper) ved koloskopi vil utløse behov for kontroll-koloskopier. Ventelistene for koloskopi har vært lange i en årrekke og har kommet opp i 100 uker på ett av våre Universitetssykehus.15 Norske myndigheter har sovet i timen. Det vil ta flere år før endoskopikapasiteten er i nærheten av hva den må være for at screening for KRK kan innføres i Norge. FIT-screening ble nylig introdusert i Danmark og Nederland. I begge land førte innføring av screening til en enorm overbelastning av endoskopikapasiteten og økte ventetider for pasienter med symptomer og behov for utredning. På alle måter er dette en uakseptabel situasjon. Vi må aldri sette oss i den situasjonen at vi undersøker friske personer uten symptomer på bekostning av pasienter med symptomer på sykdom. Det er nylig nedsatt et midlertidig fagråd i Helse Sør-Øst som blant annet skal se på fremtidig behov for koloskopi. Det er på høy tid.
Referanser
1. Cancer Registry of Norway. Cancer in Norway 2011 – Cancer incidence, mortality, survival and prevalence in Norway. Oslo: Cancer Registry of Norway; 2013.
2. Muto T, Bussey HJ, Morson BC. The evolution of cancer of the colon and rectum. Cancer 1975;36:2251-70.
3. http://www.cancerscreening.nhs.uk/bowel/. (Accessed Dec 3rd 2013, at http://www.cancerscreening.nhs.uk/bowel/.)
4. Holme O, Bretthauer M, Fretheim A, Odgaard-Jensen J, Hoff G. Flexible sigmoidoscopy versus faecal occult blood testing for colorectal cancer screening in asymptomatic individuals. Cochrane Database Syst Rev 2013;In press.
5. van Dam L, Kuipers EJ, van Leerdam ME. Performance improvements of stool-based screening tests. Best Pract Res Clin Gastroenterol 2010;24:479-92.
6. Thiis-Evensen E, Hoff GS, Sauar J, Langmark F, Majak BM, Vatn MH. Population-based surveillance by colonoscopy: effect on the incidence of colorectal cancer. Telemark Polyp Study I. Scand J Gastroenterol 1999;34:414-20.
7. Schoen RE, Pinsky PF, Weissfeld JL, et al. Colorectal-cancer incidence and mortality with screening flexible sigmoidoscopy. N Engl J Med 2012;366:2345-57.
8. Segnan N, Armaroli P, Bonelli L, et al. Once-only sigmoidoscopy in colorectal cancer screening: follow-up findings of the Italian Randomized Controlled Trial–SCORE. J Natl Cancer Inst 2011;103:1310-22.
9. Holme O, Loberg M, Kalager M, et al. Effect of flexible sigmoidoscopy screening on colorectal cancer incidence and mortality: a randomized clinical trial. JAMA 2014;312:606-15.
10. Atkin WS, Edwards R, Kralj-Hans I, et al. Once-only flexible sigmoidoscopy screening in prevention of colorectal cancer: a multicentre randomised controlled trial. Lancet 2010;375:1624-33.
11. Cancer Registry of Norway. Bowel Cancer Screening in Norway – a pilot study. (Accessed October 29th, 2014, at http://www.kreftregisteret.no/en/Cancer-prevention/Screening-for-colorectal-cancer/.)
12. Lansdorp-Vogelaar I, Knudsen AB, Brenner H. Cost-effectiveness of colorectal cancer screening – an overview. Best Pract Res Clin Gastroenterol 2010;24:439-49.
13. Kaminski MF, Bretthauer M, Zauber AG, et al. The NordICC Study: rationale and design of a randomized trial on colonoscopy screening for colorectal cancer. Endoscopy 2012;44:695-702.
14. Brenner H, Stock C, Hoffmeister M. Effect of screening sigmoidoscopy and screening colonoscopy on colorectal cancer incidence and mortality: systematic review and meta-analysis of randomised controlled trials and observational studies. BMJ 2014;348:g2467.
15. Aftenposten Aug 21st 2014: Inntil 100 ukers ventetid for tarmundersøkelse. 2014. (Accessed Nov 17th, 2014, at http://www.aftenposten.no/nyheter/iriks/Inntil-100-ukers-ventetid-for-tarmundersokelse-7675371.html.)
16. Whitlock EP, Lin JS, Liles E, Beil TL, Fu R. Screening for colorectal cancer: a targeted, updated systematic review for the U.S. Preventive Services Task Force. Ann Intern Med 2008;149:638-58.
17. Imperiale TF, Ransohoff DF, Itzkowitz SH. Multitarget stool DNA testing for colorectal-cancer screening. N Engl J Med 2014;371:187-8.
18. Gandon Y. Screening for colorectal cancer: the role of CT colonography. Diagnostic and interventional imaging 2014;95:467-74.
19. Spada C, Hassan C, Galmiche JP, et al. Colon capsule endoscopy: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2012;44:527-36.