Klinikk
Kreft og venøs trombose
Anders Erik Astrup Dahm, Hematolog, overlege og førsteamanuensis ved Akershus universitetssykehus og Institutt for klinisk medisin, Universitetet i Oslo
Forekomsten av venøs trombose hos kreftpasienter varierer fra 2-20% per år (1). Til sammenlikning er forekomsten i den alminnelige norske befolkningen ca. 2/1000 per år. Det er derfor meningsfullt å vurdere tromboseprofylakse hos alle kreftpasienter.
Tromboseprofylakse
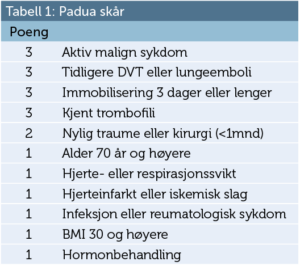
Padua skår er en skår for å bestemme hvilke indremedisinske pasienter som bør få tromboseprofylakse (2). Får man mer enn 4 poeng er det anbefalt å gi tromboseprofylakse. I denne skåren gir enhver kreftsykdom 3 poeng. Det betyr i praksis at nesten alle kreftpasienter som legges inn med akutt sykdom bør få tromboseprofylakse. (Tabell 1).
Blant polikliniske kreftpasienter bør de med høy risiko for venøs trombose få tromboseprofylakse. Det er vist at å gi tromboseprofylakse til en uselektert populasjon av polikliniske kreftpasienter vil gi et for høyt «Numbers needed to treat» (NNT) til at det regnes som effektivt (3, 4). Men hvis man bruker en risikoskår til å plukke ut pasienter med høy risiko gir det lavere NNT (5, 6). Den risikoskåren som er best dokumentert og som også er enkel å bruke er Khorana skår (7). Hos kreftpasienter som skal få kjemoterapi og som får 2 poeng i Khorana skår kan man da gi tromboseprofylakse. Dessverre er det kun lavmolekylært heparin som har dette som godkjent indikasjon, DOAK kan derfor ikke brukes selv om det er vist at det virker. (Tabell 2).
Behandling av venøs trombose hos kreftpasienter
De fleste kreftpasienter som får venøs trombose kan behandles med en av de direktevirkende orale faktor Xa hemmerne edoksaban, rivaroksaban, eller apiksaban (8-10). Trombinhemmeren dabigatran er ikke testet ut hos kreftpasienter og anbefales derfor ikke. Alle kreftpasienter kan også behandles med lavmolekylært heparin for sin venøse trombose, mens warfarin regnes som dårligere siden det gir hyppigere residivtromboser. Dalteparin er det lavmolekylære heparinet som er best dokumentert hos kreftpasienter i Norge brukes dalteparin og enoksaparin om hverandre uten at vi kan si at det ene er bedre eller dårligere enn det andre.
Gastrointestinal og urologisk kreft
Både edoksaban og rivaroksaban gir flere store blødninger enn lavmolekyært heparin hos pasienter med gastrointestinal kreft. I studiene av apiksaban sees ikke denne forskjellen. Derimot så observerte man at pasienter med resesert gastrointestinal kreft ikke fikk noe særlig blødninger i det hele tatt (11, 12). Det har også vært antydet at pasienter med urologisk kreft har flere store blødninger på edoksaban enn lavmolekylært heparin, men det er små tall som underbygger dette og tilsvarende stor usikkerhet. I studiene av apiksaban så ser det ut til at pasienter med urologisk kreft blødde mye uansett om de fikk behandling med apiksaban eller lavmolekylært heparin.
Kreftpasienter med høy risiko for blødning
Pasienter med høy risiko for blødning bør behandles med lavmolekylært heparin så lenge de er blødningsutsatt. Grunnen er at lavmolekylært heparin har kortere halveringstid enn DOAK, det finnes antidot (protaminsulfat) og det er lettere å redusere dosen siden det er flere dosetrinn. Hvilke pasienter som har høy risiko for blødning er en klinisk vurdering. Eksempler er pasienter med luminale svulster, trombocytopeni under 50, eller klinisk blødningstendens. Lav Hb uten forklaring før oppstart av antikoagulasjon kan være et tegn på en liten uoppdaget blødning, som kan bli forverret når man starter antikoagulasjon.
Behandlingslengde
Kreftpasienter skal som hovedregel behandles i 6 måneder for sin venøse trombose eller så lenge de har kreft. Behandling i den palliative fasen må sees i lys av den eventuelle symptomlindring antikoagulasjon kan gi, f.eks. ved tungpustenhet som skyldes lungeemboli. Hvis ikke antikoagulasjon gir symptomlindring er det ikke hensiktsmessig å gi det i den palliative fasen. Brystkreftpasienter som har fått venøs trombose og som behandles langvarig med tamoksifen bør sannsynligvis bruke antikoagulasjon så lenge de bruker tamoksifen.
Dosereduksjon av antikoagulasjon
Lavmolekylært heparin dosereduseres rutinemessig til 150 E/kg x 1 etter 4 ukers behandling. Ved behandling med DOAK er det foreløpig kun én publisert studie som har testet ut dosereduksjon (13). I denne enarmede intervensjonsstudien ble apiksaban doseredusert til 2.5 mg x 2 etter 6 måneder hos de som ikke allerede hadde fått residiv av venøs trombose eller alvorlig blødning. Det ble observert få residivtromboser og få alvorlige blødninger i de neste 30 månedene etter dosereduksjon, slik at dette regimet er trolig trygt å bruke i denne pasientgruppen.
Medikamentinteraksjoner
Lavmolekylært heparin har i praksis ingen medikamentinteraksjoner utover andre medikamenter som også gir blødningstendens, f.eks. blodplatehemmere og NSAID. DOAK påvirkes av medikamenter som induserer eller hemmer CYP3A4 og P-glykoprotein. Rivaroksaban og apiksaban metaboliseres av begge disse enzymene, mens edoksaban kun er avhengig av P-glykoprotein. Imidlertid er det ofte slik at medikamenter som påvirker CYP3A4 også ofte påvirker P-glykoprotein, dermed er det de samme medikamentene som interagerer med alle DOAK’ene. En sjelden gang i blant kan det være pasienter som ikke kan bruke rivaroksaban eller apiksaban grunnet medikamentinteraksjoner som likevel kan bruke edoksaban. Det er nesten ingen studier som har studert medikamentinteraksjoners effekt på kliniske endepunkter, slik at dette er hovedsakelig teoretiske overveininger. Eksempler på kreftmedisiner som interagerer med DOAK er dabrafenib, enzalutumid og idelalisib.
Svulst i hjernen
Det er veldig lite data på DOAK behandling av venøs trombose hos pasienter med primær eller metastatisk hjernesvulst. De få studiene som er gjort er utelukkende gjennomganger av historiske data. Det er derfor vanskelig å si om DOAK kan brukes ved intracerebrale svulster. De fleste leger vil nok foretrekke lavmolekylært heparin fordi det har kortere halveringstid og det finnes antidot.
Nyresvikt
Nyresvikt påvirker utskillelse av både lavmolekylært heparin og DOAK. For lavmolekylært heparin kan det være nyttig å styre behandlingen etter anti-faktor Xa aktivitet hos disse pasientene. Ved behandling med DOAK må man være forsiktig ved kreatinin-clearence under 30 og dosereduksjon kan være nødvendig, se preparatomtalene av medikamentene. Det vil også være nyttig å holde øye med klinisk blødningstendens hos disse pasientene.
Oppsummering
De orale faktor Xa hemmerne kan brukes til de fleste kreftpasienter med venøs trombose, selv om det i perioder med biopsier, operasjoner og andre inngrep vil være nødvendig å bruke lavmolekylært heparin. Apiksaban gir ikke mer alvorlig blødning enn lavmolekylært heparin hos pasienter med gastrointestinal kreft, i hvert fall ikke når tumor er operert bort. Husk å vurdere alle inneliggende kreftpasienter for tromboseprofylakse med Padua skår og polikliniske pasienter med Khorana skår.
Referanser
1. Cohen AT, Katholing A, Rietbrock S, Bamber L, Martinez C. Epidemiology of first and recurrent venous thromboembolism in patients with active cancer. A population-based cohort study. Thromb Haemost. 2017;117(1):57-65.
2. Barbar S, Noventa F, Rossetto V, Ferrari A, Brandolin B, Perlati M, et al. A risk assessment model for the identification of hospitalized medical patients at risk for venous thromboembolism: the Padua Prediction Score. J Thromb Haemost. 2010;8(11):2450-7.
3. Agnelli G, George DJ, Kakkar AK, Fisher W, Lassen MR, Mismetti P, et al. Semuloparin for thromboprophylaxis in patients receiving chemotherapy for cancer. The New England journal of medicine. 2012;366(7):601-9.
4. Agnelli G, Gussoni G, Bianchini C, Verso M, Mandala M, Cavanna L, et al. Nadroparin for the prevention of thromboembolic events in ambulatory patients with metastatic or locally advanced solid cancer receiving chemotherapy: a randomised, placebo-controlled, double-blind study. Lancet Oncol. 2009;10(10):943-9.
5. Khorana AA, Soff GA, Kakkar AK, Vadhan-Raj S, Riess H, Wun T, et al. Rivaroxaban for Thromboprophylaxis in High-Risk Ambulatory Patients with Cancer. The New England journal of medicine. 2019;380(8):720-8.
6. Carrier M, Abou-Nassar K, Mallick R, Tagalakis V, Shivakumar S, Schattner A, et al. Apixaban to Prevent Venous Thromboembolism in Patients with Cancer. The New England journal of medicine. 2019;380(8):711-9.
7. Khorana AA, Kuderer NM, Culakova E, Lyman GH, Francis CW. Development and validation of a predictive model for chemotherapy-associated thrombosis. Blood. 2008;111(10):4902-7.
8. Raskob GE, van Es N, Verhamme P, Carrier M, Di Nisio M, Garcia D, et al. Edoxaban for the Treatment of Cancer-Associated Venous Thromboembolism. The New England journal of medicine. 2018;378(7):615-24.
9. Young AM, Marshall A, Thirlwall J, Chapman O, Lokare A, Hill C, et al. Comparison of an Oral Factor Xa Inhibitor With Low Molecular Weight Heparin in Patients With Cancer With Venous Thromboembolism: Results of a Randomized Trial (SELECT-D). J Clin Oncol. 2018;36(20):2017-23.
10. Agnelli G, Becattini C, Meyer G, Muñoz A, Huisman MV, Connors JM, et al. Apixaban for the Treatment of Venous Thromboembolism Associated with Cancer. The New England journal of medicine. 2020;382(17):1599-607.
11. Ageno W, Vedovati MC, Cohen A, Huisman M, Bauersachs R, Gussoni G, et al. Bleeding with Apixaban and Dalteparin in Patients with Cancer-Associated Venous Thromboembolism: Results from the Caravaggio Study. Thromb Haemost. 2020.
12. Hussaini P, Larsen TL, Ghanima W, Dahm AEA. Risk Factors for Bleeding in Cancer Patients Treated with Conventional Dose Followed by Low-Dose Apixaban for Venous Thromboembolism. Thromb Haemost. 2023