Utdanning og møter
ESMO 2023: Nytt om uro-onkologisk kreft
Maria Nyre Vigmostad, Spesialist i onkologi, Avdeling for blod- og kreftsjukdommar, Stavanger Universitetssjukehus
Introduksjon:
ESMO 2023 var konferansen då me fekk oppleve plystring, ståande applaus og tårer på hovudsesjon for ein urologisk cancer. Dei fantastiske blærekreftresultata fekk sindige onkologar til å reagere med glade tilrop og optimisme på vegne av ei ofte underbehandla gruppe pasientar med dårleg prognose. Det var sjølvsagt nyheiter innan andre urologiske kreftformer også, og under kjem eit samandrag av det viktigaste frå konferansen sett frå ein uro-onkolog sin ståstad.
Blærekreft:
Behandling av metastatisk blærekreft var uforandra i fleire tiår fram til 2020; Kjemoterapi med gemcitabin og cisplatin (eventuelt carboplatin). Median overlevelse låg på omlag 14 månader. Data frå Javelin-bladder 100 studien blei lagt fram på virtuell ASCO i 2020(1). I denne studien fekk pasientar som ikkje progredierte på standard kjemoterapi, vedlikehaldsbehandling i etterkant med immunterapi (avelumab). Median overlevelse steig då til i overkant av 21 månader. Karismatiske Thomas Powles som også presenterte i 2020, fekk i år lov til å legge fram banebrytande resultat framfor 8000 tilhøyrarar på fellessesjon på ESMO. Det var to blærekreftstudiar som blei presentert i same fellessesjon.
EV 302 (LBA6)
I fase 3-studien EV 302 blei pasientar med tidlegare ubehandla metastatisk blærekreft randomisert 1:1 til enten platinumbasert kjemoterapi med gemcitabin og cisplatin (eller carboplatin) i seks syklusar, eller enfortumab vedotin (EV) dag 1 og 8 og pembrolizumab dag 1. EV blei gitt til progresjon og pembrolizumab i maksimalt 2 år. Hovudendepunkt var progresjonsfri overlevelse (PFS) og total overlevelse (OS).
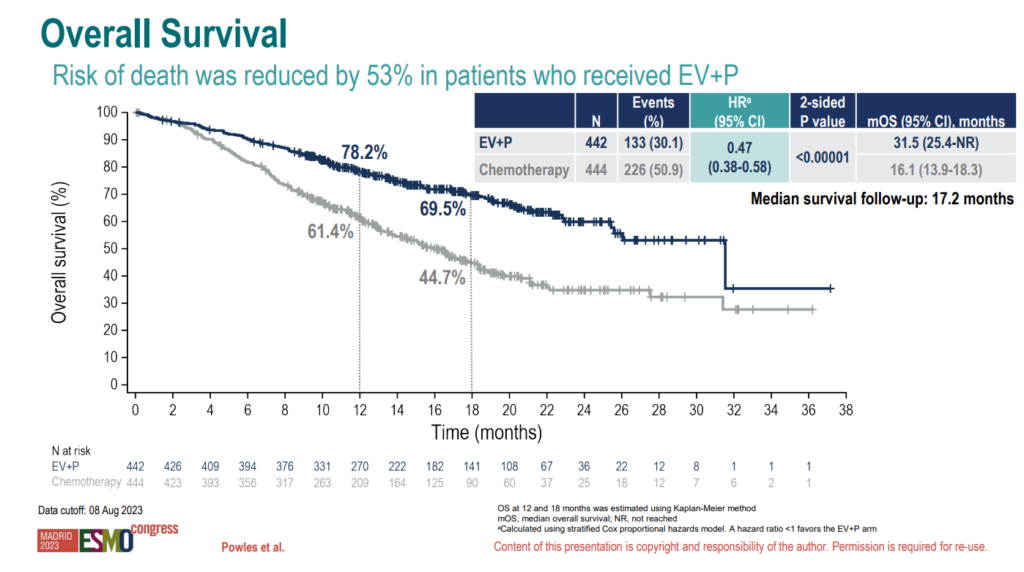
Knapt 900 pasientar blei randomisert. Det var ei nesten dobling av OS med median i EV+ pembrolizumab arm på 31.5 månader mot 16.1 månader i kjemoterapiarmen (HR 0.47, p<0.00001). Ein såg effekt av EV + pembrolizumab over alle subgrupper og fordelen var uavhengig av PDL1 status, viscerale metastasar eller ikkje, og av om pasienten var cisplatinkandidat eller ei.
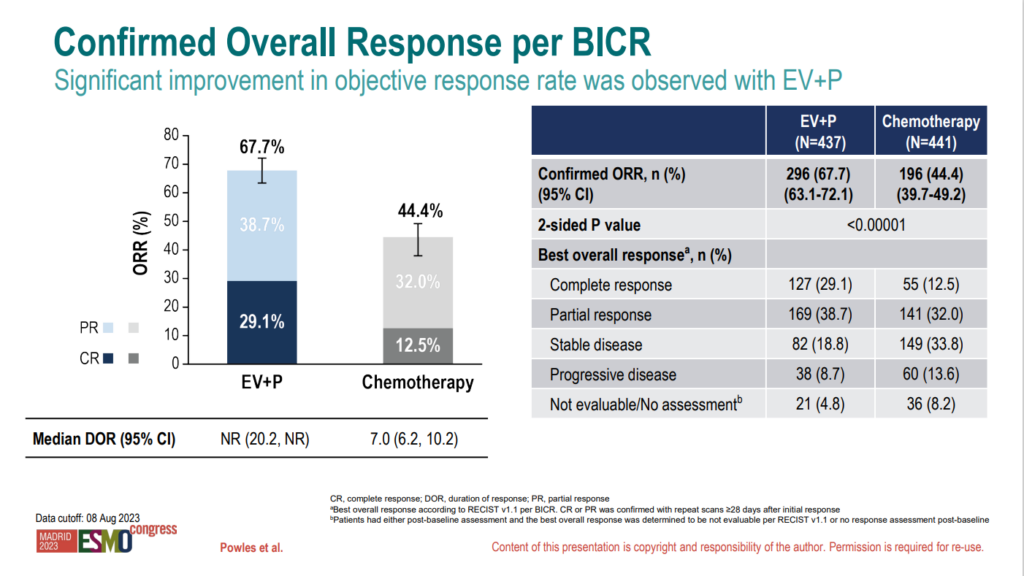
Responsraten var høg; 68% mot 44% i kjemoterapiarmen. I tillegg såg ein 29% komplette responsar mot 12% i standardarmen. Det ser ut som den høge delen komplette responsar saman med lang varigheit på respons (median ikkje nådd mot 7 månader) er det som driv overlevelsesgevinsten.
Enfortumab vedotin er eit antistoff medikament konjugat (ADC) som bind seg til nectin4 som er uttrykt på urotel celler. Nectin 4 er også overuttrykt mellom anna i hud og forklarer at 67% av pasientane hadde hudbiverknader- grad III i 15% av tilfella. 63% av pasientane fekk nevropati mot 30% i kontrollarmen (grad III 7 mot 0%). Totalt var det likevel færre grad III biverknader hos pasientar som fekk EV + pembrolizumab versus kjemoterapi (56 mot 69%).
Checkmate 901 (LBA7)
To negative fase 3-studiar har allereie undersøkt om immunterapi i tillegg til platinumbasert kjemoterapi har effekt på overlevelse i fyrstelinjebehandling av metastatisk blærekreft(2, 3). Desse studiane inkluderte også pasientar som ikkje kunne få cisplatin. Fase 3-studien Checkmate 901 blei også presentert i fellessesjon. Denne studien inkluderte berre pasientar som var aktuelle for cisplatinbehandling i fyrstelinjebehandling av metastatisk blærekreft. Pasientane fekk enten gemcitabin og cisplatin (GC) opp mot 6 syklusar, eller GC opp mot 6 syklusar + nivolumab opp mot 2 år. Hovudendepunkt var PFS og OS.
Det var omtrent 300 pasientar i kvar arm. Det var signifikant betre OS med median på knapt 22 månader mot 19 månader (HR 0.78, p=0.0171) og dette såg ein for alle subgrupper.
Objektiv responsrate var 58% i den eksperimentelle armen mot 43% i GC armen. Median responslengde var også forbetra; 37 mot 12 månader. Ein såg 22% komplette responsar i den eksperimentelle armen mot 11% i GC armen.
Konklusjon blærekreft:
EV+ pembrolizumab er ny fyrstelinjebehandling for metastatisk blærekreft, med ein auke i median OS til over 31 månader. EV + pembrolizumab har best responsrate og er betre tolerert. Per i dag er behandlinga ikkje godkjent verken i EMA eller i Norge. Eit samla miljø ser fram til den dagen me kan tilby dette til våre pasientar!
Frå Checkmate 901 kan ein konkludere at for pasientar som er kandidatar for cisplatin, så har både sekvensiell immunterapi (etter Javelin bladder-100) og kombinasjonsbehandling (Checkmate 901) overlevelsesgevinst. Også her ventar me på norsk godkjenning.
Prostatakreft
Enza-p (LBA84)
Dette er ein fase 2-studie som undersøkte tillegg av LuPSMA til nyare hormonbehandling (NHA) med enzalutamid for metastatisk kastrasjonsresistent prostatakreft (mCRPC). Pasientane skulle ikkje tidlegare ha fått kjemoterapi eller hormonbehandling for mCRPC, og skulle ha minst to risikofaktorar som gav auka risiko for at enzalutamid aleine skulle feile (t.d.: >LD, >ALP, <albumin mm). Pasientane fekk enten enzalutamid aleine eller enzalutamid med tillegg av LuPSMA 2-4 behandlingar avhengig av opptak på interim PET. Primære endepunkt var PSA-PFS.
Det var om lag 80 pasientar i kvar arm og PSA-PFS var lengre med enzalutamid-LuPSMA versus enzalutamid aleine, med median på 13 mot 8 mnd (HR 0.43, p=0.00001). Ein såg ingen auke i rapporterte biverknader i den eksperimentelle armen, og kanskje det skuldast den adaptive doseringa. Meir kan sjå ut til å vera betre for enkelte, og i såfall er pasientseleksjon nøkkelen. Godkjente behandlingar for mCRPC er uansett basert på gevinst i total overlevelse. Ein venter overlevelsesdata frå denne studien medio 2024.
PSMA fore (LBA13)
Fase 3-studien PSMA-fore inkluderte pasientar med mCRPC som skulle ha progrediert på ei linje med NHA. Primære endepunkt var PFS og OS.
Knapt 500 pasientar blei randomisert til enten endring av NHA eller behandling med LuPSMA kvar 6. veke i totalt seks syklusar. 85% av pasientane kryssa over til LuPSMA-armen. Det var signifikant betring i PFS med median i eksperimentell arm på 12 månader mot knapt 6 månader i NHA-arm (HR 0.43). Median OS i analyse justert for overkrysning var lik (19.25 mot 19.55), og i den ikkje-justerte var median OS 19.25 mot 19.71 med HR på 1.16.
Kontrollarmen er problematisk og ein veit frå andre studiar at å endre NHA kan samanliknast med placebo(4, 5). Studien gir data på bruk før docetaxel, men fortel lite om når LuPSMA skal brukast og basert på denne studien erstattar ikkje LuPSMA eksisterande val. Andre studiar har allereie vist at LuPSMA er ei effektiv behandling som gir betring i overlevelse(6).
ProBio (LBA86)
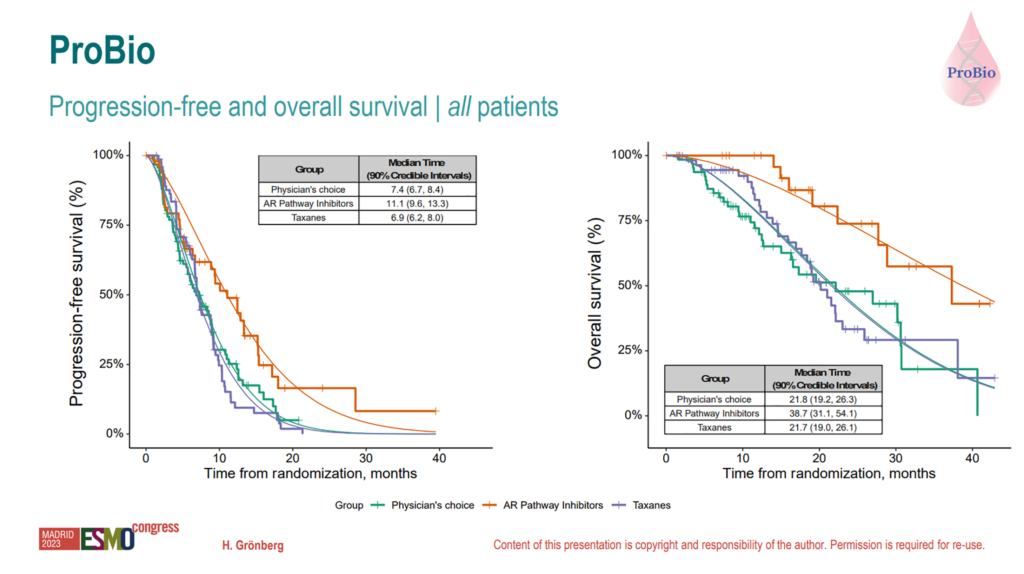
Fleire sjukehus i Norge inkluderer i ProBio studien. ProBio er ein biomarkørdriven, randomisert, adaptiv plattformstudie for pasientar med metastatisk prostatakreft. Ein samanliknar biomarkørdriven seleksjon av behandling mot legen sitt val av standard behandling. På ESMO blei det presentert data for fyrstelinjebehandling av mCRPC med PFS og OS som primære endepunkt.
219 pasientar blei randomisert og det var ei klar forbetring av median OS for biomarkørdriven NHA (11 månader) versus taksaner (7 månader) og legen sitt val av standardbehandling (7.5 månader). Effekten er stort sett driven av androgenreseptor og tp53 villtype.
Studien støttar praksis siste åra; NHA er føretrekke framfor taksaner i fyrstelinjebehandling av mCRPC.
Nyrecellekreft
Hif2-α er ein hovuddrivar i Von Hippel Lindau og klarcella nyrekreft, og det var fleire studiar på hif2-α hemmaren belzutifan som blei presentert på årets ESMO.
I fase 3-studien Litespark 005 (LBA88) samanlikna ein behandling med belzutifan mot everolimus i seinare linjer av metastatisk, klarcella nyrecellekreft. I overkant av 700 pasientar ble inkludert og primære endepunkt var PFS og OS.
Pasientane skulle ha fått 1-3 tidlegare behandlingslinjer inkludert immunterapi, og for >85% så var dette 3. eller 4. linjes behandling. Studien var positiv for PFS (HR 0.75, p<0.01), men utan signifikant betring i total overlevelse. Responsraten i denne tungt behandla gruppa var 23% for belzutifan mot 3.5% for everolimus. Det var 62% grad III biverknader i begge armane, og >80% av pasientane som fekk belzutifan hadde anemi (grad III hos 32%).
Utan betring i overlevelse så er det vanskeleg å seie at dette er praksisendrande resultat. Men det manglar fase 3-studiar med OS gevinst etter immunterapi i så seine behandlingslinjer, og utifrå det perspektivet så er dette velkomne data.
Hif2-α hemmar er nok på veg inn, men kanskje fortrinnsvis i tidlegare linjer. Data blei også presentert på konferansen frå fase 2-studien Litespark 003 (LBA87); her var responsraten på nesten 70% for kombinasjonen av belzutifan og cabozantinib hos tidlegare behandlingsnaive pasientar med metastatisk, klarcella nyrecellekreft.
Testikkelkreft
Øivind Kvammen, overlege PhD frå Ålesund, presenterte poster på pasientar med testikkelkreft. Posteren var basert på journalgjennomgang av 558 avdøde pasientar med testikkelkreftdiagnose frå 1980-2009. Hovudfokus var å karakterisere pasientar som døyde av testikkelkreft eller av behandlinga. Ein såg behandlingsrelaterte dødsfall hos 41/588 pasientar. Over 90% av desse fekk kjemoterapi og døyde som komplikasjon til dette. Dødsfall av testikkelkreft var svært sjeldan ved klinisk stadium 1 eller ved IGCCCG god prognosegruppe, og hyppigast for dei med non-seminom, viscerale metastasar eller dersom det var behov for ytterlegare kjemoterapi i etterkant av kirurgi. Dette er del av eit stort arbeid ein gjer for å identifisere risikofaktorar som ytterlegare kan redusere dødelegheit av testikkelkreft eller behandling.