Av Torjan Magne Haslerud. Overlege, Haukeland Universitets Sykehus
Innledning
Selektiv intern radioterapi (SIRT) eller radioembolisasjon (RE) er en lokal-stråleterapi for primære og sekundære levertumores. Metoden ble utviklet i Australia på slutten av 80-tallet og har vært godkjent til klinisk bruk i Europa siden 2003. Virkeprinsippet i denne behandlingen er at små radioaktive (Yttrium-90) mikrosfærer akkumuleres ilevermetastaser/-tumores og bestråler disse innenfra. Dette oppnås ved injeksjon av Y-90-mikrosfærene i lever- og tumorarterier via mikrokateter. De radioaktive mikrosfærene er cirka 20-60 µm i diameter og blir hengende igjen i arterioler og kapillarer. Terapisubstansen injiseres arterielt, da levertumores og –metastaser hovedsakelig er arterielt perfundert (ca. 90-99%), mens det normale leverparenkymet forsørges i største grad av portal-venen (ca. 80%). I tillegg har levertumores ofte en utpreget hyperperfusjon og angioneogenese, som igjen medfører at radioaktiviteten så å si suges inn i kapillar-redene svulstene danner. Kombinasjonen av strålerekkevidden til Y-90 (maks 11 mm i vev) og de ovennevnte perfusjonsforholdene resulterer i at en intratumoral stråledose på gjennomsnittlig 200-600 Gy (delvis >1000 Gy) kan oppnås. De samme egenskapene medfører også en limitering av stråledosen for det normale leverparenkymet til et tolerabelt nivå.
Behandlingen er en multidisiplinær behandling, som forutsetter flinke intervensjons-radiologer samt erfarne onkologer, kirurger, nukleærmedisinere og strålefysikere for å sikre en god og korrekt terapi for pasientene.
Bilde 1. Helkroppscintigrafi (Tc99m-MAA-simulering): Høyre bilde: selektivt opptak i levermetastasene (mCRC) med redusert opptak i normalt levervev. Venstre bilde (samme pasient): oppjustert intensitet for bedømming av ekstrahepatiske opptak (ingen påvist) og bedømming av lungeshunt. Lett til moderat diffust Tc-opptak ses i begge lunger, som ble beregnet til 7% og var dermed ikke relevant for behandlingen (ingen kontraindikasjon eller dosereduksjon nødvendig).
Bilde 2.Pasient med levertumor (metastase fra CRC) i venstre leverlapp og diffust Tc-opptak i begge lunger grunnet relevant lungeshunt (beregnet til 17%). En lungeshunt under 20 %, men over 10% fører til en obligatorisk dosereduksjon av beregnet terapiaktivitet.
Indikasjoner:
Det eksisterer forskjellige kliniske situasjoner, hvor SIRT kan være en behandlingsopsjon. Behandlingen kan gjennomføres både på levermetastaser og på primær leverkreft (cholangiocellulært carcinom (CCC) og hepatocellulært carcinom (HCC) ). Forutsetningene er at det foreligger en inoperabel situasjon og eventuelt mangel på andre terapialternativer (f.eks. kjemoresistens). I tillegg skal pasientene være i god almenntilstand, ha forventet levetid på over 3 måneder, god leverfunksjon og den hepatiske tumorlasten skal være prognoseavgjørende.
De hyppigste indikasjonene er siste linjes behandling for mCRC og metastaseterapi ved kjemoresistens eller –intoleranse, hvor behandlingen også nevnes i ESMOs guidelines. Metoden kan også gjennomføres på en rekke andre tumorentiteter med levermetastaser (f.eks. mammacancer, GIST, andre GI-cancere). Øvrige behandlingssituasjoner er ved HCC, enten som en ren palliativ terapi, Bridging til levertransplantasjon eller pre-operativ behandling av HCC. I sistnevnte situasjon kan man ved hjelp av SIRT oppnå lokal tumorkontroll og samtidig hypertrofi av kontralateral lapp, dersom det er tvilsomt om det postoperativt ville vært tilstrekkelig normalt levervev igjen. I tillegg kan behandlingen være nyttig for pasienter med nevroendocrine tumores (NET), enten ved Somatostatin reseptor (SSTR) -negative levermetastaser eller for å dempe symptomene fra hyper-sekretoriske/hormon produserende NET ved leverdominant sykdom.
Planlegging av SIRT:
Før gjennomføring av en SIRT-behandling anbefales at kandidaten blir diskutert på et MDT-møte. Dette for å avklare indikasjon, operabilitet, eventuelt bedre terapiopsjoner, samt for å verifisere at det ikke foreligger kontraindikasjoner hverken for SIRT eller angiografi.
Kontraindikasjoner for SIRT er redusert leverfunksjon (spesielt høye Bilirubin-verdier, ascites, lav Albumin), tidligere strålebehandling av lever, dårlig allmenntilstand, relevant ekstrahepatisk sykdom, hepatisk tumorlast på over 70% og lungeshunting over 20 %.
Dersom det ikke foreligger kontraindikasjoner, anbefales ofte at en FDG-PET/CT (bilde 5) gjennomføres før behandling. Undersøkelsen brukes som baseline-undersøkelse, til å utelukke ekstrahepatisk sykdom samt for kartlegging av vital, hepatisk tumorlast. Flere behandlingsentre velger å utføre MR-lever eller 3-fase-CT-lever for kartlegging av hepatisk tumorlast og som follow up. Fordelen med FDG-PET/CT er at man ser en tidlig metabolsk respons, som igjen er en god prediktor for overlevelse [9]
Bilde 3. (SPECT/CT fra terapisimulering): Viser høyt opptak av testsubstansen (Tc-99m-MAA) i en levermetastase i venstre leverlapp) med ønsket redusert opptak i friskt leverparenkym.
Bilde 4. (FDG-PET/CT 4 uker etter (øvre rekke) SIRT og før SIRT (nedre rekke): MIP-bildet helt til venstre viser en metabolsk partiell remisjon av levermetastasene (mCRC) etter SIRT. Snittbildene (de tre øvrige) viser eksempelvis en metabolsk komplett remisjon av samme levermetastase, som viser økt Tc-opptak i bilde 3. Lenger lateralt i venstre leverlapp sees en partiell remisjon.
Gjennomføring av terapisimulering:
Pasienten går først gjennom en terapi-simulering (s. bilde 1-3). I denne simuleringen kartlegges, ved hjelp av angiografi, leverkar-anatomi og øvrige kar, som forsørger nærliggende organer, spesielt er man oppmerksom på arterier som går til magesekk, pankreas og tynntarm. En «ufarlig» test-substans (Tc-99m-MAA) blir injisert i de arterie-posisjonene, som en har tenkt å injisere Y-90-mikrosfærene i. Denne test-substansen oppfører seg omtrent som Y-90-mikrosfærene in vivo og kan dermed brukes som kartlegging om pasienten er en kandidat for SIRT (s. bilde 3 og 4). Etter angiografien tas en helkroppsscintigrafi og SPECT/CT-abdomen på nukleærmedisinsk avdeling for å se på fordeling av testsubstansen i lever og kroppen for øvrig (s. bilder 1-6). Dette gjøres hovedsakelig for å detektere eventuell ekstrahepatisk tracerdeposisjon og beregne lungeshunt (s. bilde 1 og 2), men også for å verifisere om en har selektivt traceropptak i levermetastasene (s. bilder 3-6).
Dersom ekstrahepatiske opptak påvises, må en eventuell aksessorisk arterie lokaliseres og coiles i en ny MAA-testsimulering. Lykkes det ikke å identifisere arterien, kan behandlingen ikke gjennomføres. Dersom man behandler på tross av ekstrahepatisk deposisjon kan stråleulcera oppstå, som igjen er vanskelige å behandle. Påvises det en lungeshunt på > 20 % er det heller ikke mulig å gjennomføre SIRT-behandlingen grunnet økt risiko for strålepneumonitt samt fare for ikke adekvat stråledose til tumor.
Hvis MAA- og prøveangiografien ikke viser noen kontraindikasjoner, kan SIRT-behandlingen planlegges. Det er essensielt at injiseres Y-90-mikrosfærene i eksakt de samme posisjonene som man har gjennomført MAA-simuleringen i. Ellers består fare for inadekvat stråledose til levermetastasene samt muligens høyere risiko for ekstrahepatisk deposisjon, som igjen kan medføre stråleulcera.
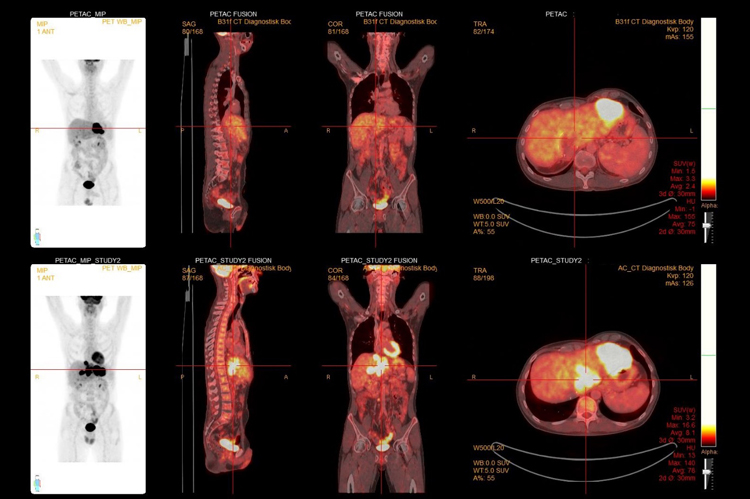
Bilde 5.(Pre-terapeutisk FDG-PET/CT): I venstre leverlapp sees uttalt metastasering fra CRC. For øvrig sees enkelte levermetastaser i begge leverlapper. Ingen relevant ekstrahepatisk sykdom sees.
Bilde 6. (Tc99m-MAA-SPECT/CT): Samme pasient som på bilde 5. SPECT/CT-bilder fra terapisimulering som viser intenst Tc-opptak i metastaser i venstre leverlapp, men også fokalt Tc-opptak i en annen levermetastase ventralt i segment 4A. I tillegg sees tydelig redusert Tc-opptak i friskt leverparenkym. Bildet viser sammenholdt med FDG-PET/CT i bilde 5 en ideell terapisituasjon.
Gjennomføring av selve SIRT-behandlingen
Under selve behandlingen injiseres mikrosfærene porsjonsvis. Hver eneste porsjon kontrolleres angiografisk. Dette både for å verifisere at kateteret ligger i korrekt posisjon og at det ikke har oppstått en endring i perfusjon. En metning av metastasene vil vise seg i en redusert perfusjon eller stase grunnet den emboliske effekten av mikrosfærene. Av og til kan også vasospasmer oppstå som igjen forårsaker stase. Det som er spesielt fryktet er retrograd perfusjon. Da er det høy fare for at mikrosfærene deponeres i andre organer, som magesekk, tynntarm eller pankreas.
En til to dager etter behandling gjennomføres enten Bremsestrålingsscintigrafi og SPECT/CT, og/eller Y-90-PET/CT (s. bilde 7). Dette er essensielt både med tanke på tumor- og leverdosimetri, det vil si fordeling av terapisubstansen intrahepatisk og at det ikke påvises ekstrahepatiske opptak. Bildeakkvireringen etter behandling kan gi en pekepinn på om man har oppnådd ønsket stråledose i tumor/-es og om en kan forvente bivirkninger i form av ulcera, dersom en påviser ekstrahepatisk deposisjon av terapisubstansen.
Bilde 7. (Y-90-PET/CT (øvre rekke) og FDG-PET/CT (nedre rekke): Samme pasient som på bilde 5 og 6. Øvre rekke viser ideell fordeling av terapisubstansen (Y-90-positron-stråling) med akkumulering i tumorvev i venstre leverlapp (bilde 7, nedre rekke). Oppløsning av Y-90-PET er relativt dårlig, da bare en liten andel av Y-90-strålingen er positron-stråling.
Bivirkninger
Selve behandlingen blir som regel godt tolerert og medfører sjeldent akutte bivirkninger. Typiske bivirkninger under og kort tid etter behandling er kvalme, leverkapselsmerter og influensa lignende symptomer, spesielt tretthet. Dersom pasienten har hatt en historie med galleveisinfeksjoner og/eller inngrep i galleveiene, anbefales antibiotika-profylakse grunnet økt risiko for post-terapeutisk cholangitt.
Sen bivirkninger kan være forhøyete leverenzymer og leversvikt. Sistnevnte er en sjelden bivirkning og kan ofte være vanskelig å skille fra tumorprogresjon. Dette er den mest alvorlige bivirkningen og er ofte en dødelig komplikasjon. En annen alvorlig bivirkning er stråleulcera som følge av ekstrahepatisk shunting. Dette betreffer som oftest magesekk, men er også sett i tarm og pankreas. Strålepneumonitt har tidligere vært en sen-bivirkning, men dette er ikke påvist etter at lungeshunting er tatt med i doseberegningen. Høy lungeshunt er et hyppigere problem med HCC-pasienter og/eller pasienter med portalvenetrombose.
Bilde 8 og 9. (FDG-PET/CT-MIP-bilder, pre-terapi venstre, post-terapi høyre): Pre- og post-terapeutisk MIP-bilde av en pasient med mCRC, som har fått gjennomført SIRT-behandling. Bildet viser en metabolsk partiell remisjon med fortsatt vitalt tumorvev lateralt i venstre leverlapp.
Terapiresultater
Ved kjemoresistent mCRC viser SIRT kontra BSC (best supportive care) eller konvensjonell terapi en overlevelse (OS) på 8,3 – 14,9 måneder mot 3,5 – 7,3 måneder for sistnevnte [1-3]. I snitt ses en respons i form av stabilisering eller remisjon hos ca 50 – 80% i denne pasient gruppen.
I den prospektive SIRFLOX-studien [4] prøves SIRT i kombinasjon med FOLFOX. Foreløpige resultater har vist en PFS i lever på 20,5 måneder for kombinasjonsbehandling mot 12,6 måneder for FOLFOX. Derimot ses ingen signifikant forskjell i total PFS (10,7 vs. 10,2 måneder. Om forskjellen i lever-PFS utgjør en signifikant endring i OS gjenstår å se, disse resultatene er ikke klare i skrivende stund. På bilde 8 og 9 vises en pasient med mCRC før og etter SIRT.
Ved HCC ses en OS på 48 måneder for SIRT kontra 32 måneder for transarteriell kjemoembolisasjon TACE som første linjes behandling ved intermediært eller avansert tumorstadium [5]. Ved avansert sykdom er OS for SIRT 16 måneder kontra 8 måneder for best supportive care (BSC) [6].
Lang overlevelse (25-70 måneder) og respons inkludert stabilisering (overall response rate (ORR) + stable disease (SD): 60 – > 90%) er sett ved NET [7]. I tillegg kan SIRT være en terapiopsjon ved progresjon etter gjennomført peptid radioreseptor terapi (PRRT) ved NET med median OS på 29 måneder og ORR på 30,4 % og stabilisering i 60,9 % av pasientene [8].
Problematisk er likevel at de fleste studiene også de ovennevnte angående overlevelse og responsrater baseres på retrospektive data. Studier med prospektive data er relativt få med lavt pasientantall.
Konklusjon: SIRT er en multidisciplinær, lokal palliativ behandlingsmetode for pasienter med levermetastaser eller primær leverkreft. I en situasjon der pasientene ikke har andre terapiopsjoner, tilbyr SIRT et godt tålt terapi-alternativ med få bivirkninger. Behandlingen kan for noen pasienter forlenge overlevelsen og øke livskvaliteten. I hvilke tilfeller og når behandlingen er mest effektiv, er fortsatt gjenstand for forskning.
Referanser
- Hendlisz A, Van den Eynde M, Peeters M et al. Phase III trial comparing protracted intravenous fluorouracil infusion alone or with yttrium-90 resin microspheres radioembolization for liver-limited metastatic colorectal cancer refractory to standard chemotherapy. Journal of Clinical Oncology 2010; 28: 3687–3694.
- Seidensticker R, Denecke T, Kraus P et al. Matched-pair comparison of radioembolization plus best supportive care versus best supportive care alone for chemotherapy refractory liver-dominant colorectal metastases. Cardiovascular and Interventional Radiology 2012; 35; 1066‒1073.
- Bester L, Meteling B, Pocock N et al. Radioembolization versus standard care of hepatic metastases: Comparative retrospective cohort study of survival outcomes and adverse events in salvage patients. Journal of Vascular and Interventional Radiology 2012; 23: 96–105.
- Gibbs P, Heinemann V, Sharma N et al. SIRFLOX: Randomized phase III trial comparing first-line mFOLFOX6 ± bevacizumab (bev) versus mFOLFOX6 + selective internal radiation therapy (SIRT) ± bev in patients (pts) with metastatic colorectal cancer (mCRC). 2015 ASCO Annual Meeting; Journal of Clinical Oncology 2015; 33 (Suppl): Abs 3502.
- de la Torre M, Buades-Mateu J, de la Rosa PA et al. A comparison of survival in patients with hepatocellular carcinoma and portal vein invasion treated by radioembolization or Sorafenib. Liver International 2016 Feb 22; ePub doi: 10.1111/liv.13098.
- D’Avola D, Iñarrairaegui M, Bilbao JI et al. A retrospective comparative analysis of the effect of Y90-radioembolization on the survival of patients with unresectable hepatocellular carcinoma. Hepato-Gastroenterology 2009; 56: 1683–1688.
- Kennedy A, Dezarn W, McNeillie P et al. Radioembolization for unresectable neuroendocrine hepatic metastases using resin 90Y-microspheres: Early results in 148 patients; Am J Clin Oncol 2008; 31: 271–279.
- Ezziddin S, Meyer C, Kohancova S et al. 90Y radioembolization after radiation exposure from peptide receptor radionuclide therapy. Journal of Nuclear Medicine 2012; 53: 1663–1669.
- Sabet A, Meyer C, Aouf A et al. Early post-treatment FDG PET predicts survival after 90Y microsphere radioembolization in liver-dominant metastatic colorectal cancer. European Journal of Nuclear Medicine and Molecular Imaging 2014; 42: 370–376