Forskning
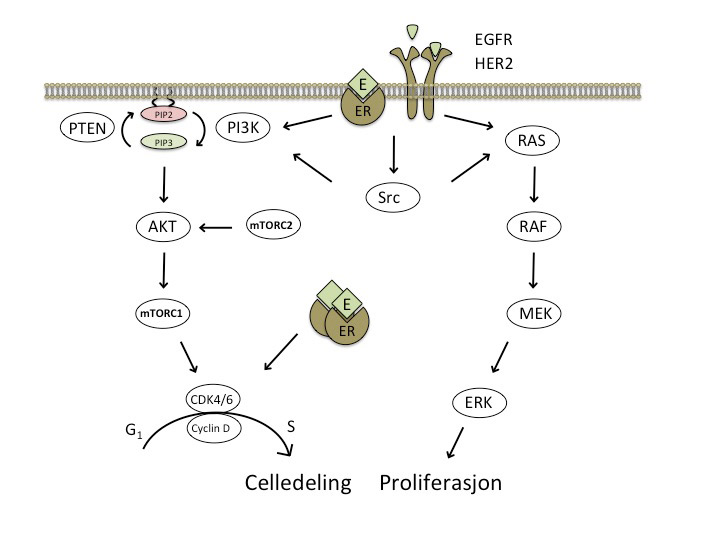
PI3K-Akt-mTOR signalering og anthracyklinresistens
Av Synnøve Yndestad1 og Hans Petter Eikesdal1,2
1 Brystkreftgruppen, Mohn kreftforskningslaboratorium, Klinisk institutt 2, Medisinsk-odontologisk fakultet,UiB.
2 Kreftavdelingen, Haukeland Universitetssjukehus
Introduksjon
Metastatisk mammacancer er fremdeles i 2014 en inkurabel sykdom, men samtidig en sykdom man kan leve med i alt fra få måneder til mange år. Især hormonreseptor (HR) positiv (østrogenreseptor (ER) og/eller progesteronreseptor (PGR) positiv) og HER2 negativ mammacancer hos pasienter med utelukkende skjellettmetastaser er en sykdom man kan leve med i mange år før behandlingsresistens utvikler seg og der man til slutt må gi tapt for sykdommen. Kunnskapen om årsaker til behandlingsresistens er etter hvert god, der man har identifisert mange ulike molekylære mekanismer [1]. Disse mekanismene spenner fra genmutasjoner til oppregulerte, vekstfremmende signalveier som gir behandlingssvikt (Figur 1). I 2013 kom der flere interessante artikler om mutasjoner i ESR1 genet (genet for østrogenreseptor), som årsak til endokrin resistens [2-4], og videre pågår det spennende studier på bruk av CDK4/6 hemmere og Src-hemmere (Figur 2) for å motvirke resistensutvikling under behandling med aromatasehemmere [1]. I Norge åpner i April 2014 MONALEESA-2 studien (fase 3, multisenter) der postmenopausale pasienter med metastatisk mammacancer randomiseres til aromatasehemmeren letrozole +/- CDK4/6-hemmeren LEE011A2301.
PI3K-Akt-mTOR signalering og endokrin resistens
Et av de store fremskritt i behandling av resistens mot endokrin terapi kom i 2012, da resultatet av BOLERO-2 studien ble publisert i New England Journal of Medicine [5]. Denne studien viser at hos postmenopausale pasienter med metastatisk mammacancer, og der sykdommen er blitt resistent mot en non-steroidal aromatasehemmer (anastrozole/letrozole), kan man forlenge progresjonsfri overlevelse betydelig dersom man skifter til den steroidale aromatasehemmeren exemestane og legger til mTOR hemmeren everolimus (Figur 2). Det er videre av interesse å merke seg at en tidligere studie der man gav mTOR hemmeren temsirolimus i 1. linje hos samme pasientpopulasjon, sammen med en aromatasehemmer, gav ingen gevinst [6], hvilket indikerer at mTOR hemmeren først gir effekt i en situasjon der resistens har utviklet seg. Det er velkjent at signalveien PI3K-Akt-mTOR hyppig er oppregulert ved brystkreft, og især ved HR positiv brystkreft [7]. Videre er aktiverende PIK3CA mutasjoner (genet for PI3K) svært hyppig i HR positiv brystkreft, som vist i store, globale analyser av brystkreftgenomet [8]. Det pågår derfor et stort antall kliniske studier der ulike hemmere av PI3K, Akt eller mTOR testes hos pasienter med brystkreft som under endokrin behandling [9]. En av disse er BELLE-3 studien der vi i Bergen og Oslo tilbyr pasienter hvor exemestane + everolimus har sviktet, skifte til fulvestrant sammen med PI3K hemmeren BKM-120/placebo (Figur 2).
PI3K-Akt-mTOR signalering og kjemoresistens
På tross av store fremskritt hva gjelder kunnskapen om resistens mot endokrin behandling, har man i liten grad applisert denne økte viten til å forbedre cellegiftbehandlingen. Cellegiftbehandling av metastatisk mammacancer er fremdeles svært viktig, og for mange pasienter den eneste behandlingsformen som stabiliserer sykdommen. Man har vist at målrettet behandling mot HER2 signalering motvirker behandlingssvikt av kjemoterapi ved HER2 amplifisert brystkreft [10], men lite er kjent om betydningen av PI3K-Akt-mTOR signalveien ved kjemoresistens [9]. Foreløpige data fra BOLERO-3 studien ble presentert på fjorårets ASCO møte i Chicago, og her studerte man effekten av trastuzumab, vinorelbine +/- everolimus ved HER2 amplifisert metastatisk mammacancer (Figur 2). Man fant en signifikant, men klinisk lite imponerende, forlengelse av progresjonsfri overlevelse fra 5.78 til 7 mndr. når everolimus ble lagt til behandlingen, hvilket enkelte har antydet kan skyldes for lav dose med everolimus på 5 mg daglig, men samtidig gav man også behandlingen uavhengig av om PI3K-Akt-mTOR signalveien var oppregulert eller ikke.
Tumor suppressorgenet PTEN er en viktig brems på PI3K-Akt-mTOR signalveien. Samtidig vet vi at PTEN inaktivering er svært vanlig ved mammacancer, især i de subgruppene der kjemoterapi er viktigste behandlingsmodalitet, slik som basalcelle-liknende brystkreft [8], og økt PI3K signalering, sekundært til PTEN inaktivering, kan derfor være av betydning ved kjemoresistens. Problemet for øyeblikket er å avklare hvilke pasienter som har oppregulert PI3K signalering. Aktiverende PIK3CA mutasjoner har vist seg lite brukende for å predikere hvem som har effekt av mTOR hemmeren everolimus, i hvert fall ved endokrin terapi i BOLERO-2 studien, som presentert på fjorårets ASCO møte. Det kan i stedet være at aktiveringsstatus av signalproteiner nedstrøms for mTOR har en høyere prediktiv verdi i denne sammenheng.
PI3K-Akt-mTOR signalering og anthracyklin resistens
Det er tidligere vist at PTEN inaktivering gir økt resistens mot anthracykliner ved brystkreft, og mTOR inhibisjon ser ut til å kunne reversere dette problemet i prekliniske brystkreftmodeller [11]. Videre er det funnet økt aktivering av Akt nedstrøms i PI3K signalveien i brystkreftceller som var doxorubicin resistente, og PI3K hemmere forsterket cytotoxiciteten av doxorubicin i disse cellelinjene [12]. Især brystkreftcellelinjen MCF-7, som er ER positiv, utviklet kraftig stigning i aktivert Akt under doxorubicinbehandling [13], hvilket kan indikere at ER positiv mammacancer er den subtypen av brystkreft der kombinasjonen av anthracykliner og PI3K hemmere har størst terapeutisk potensiale.
Vi i Brystkreftgruppen i Bergen, ledet av professor Per Eystein Lønning, har siden 1991 kjørt sammenhengende studier på ulike neoadjuvante cellegiftregimer ved lokalavansert brystkreft, og med sekvensielle biopsier tatt før, under og etter cellegiftbehandlingen. Pga. dette har vi brystkreftvev i vår biobank (RNA kvalitet) fra flere hundre pasienter med brystkreft, hvorav de fleste av dem har vært behandlet med monoterapi anthracykliner, i hele eller deler av kjemoterapiperioden. Vi har dermed et unikt materiale av brystkreftprøver hvorfra vi kan besvare hvordan PI3K-Akt-mTOR signalering påvirkes under behandlingen, og dets relasjon til respons og overlevelse.
I vårt pågående forskningsprosjekt her i Bergen studerer vi derfor i disse dager om PTEN inaktivering og PI3K-Akt-mTOR signalering er involvert i resistens mot anthracyklinene epirubicin og doxorubicin. Våre preliminære data fra de kliniske brystkreftmaterialene viser stor variasjon i PTEN og PI3K signalering mellom pasientene, og der vi finner interessante sammenhenger mellom aktiviteten i denne signalveien og kjemoterapirespons. Eksperimentelt studerer vi dette nærmere i cellekultur og i musemodeller for å besvare hvordan kjemoterapi kan kombineres med ulike hemmere av PI3K, Akt og mTOR. Håpet er at vi skal finne fram til behandlingskombinasjoner som skal gi økt effekt av kjemoterapien i fremtiden.
Referanser:
- Lonning PE, Eikesdal HP. Aromatase inhibition 2013: clinical state of the art and questions that remain to be solved. Endocr Relat Cancer 2013;20:R183-201.
- Merenbakh-Lamin K, Ben-Baruch N, Yeheskel A, Dvir A, Soussan-Gutman L, Jeselsohn R, et al. D538G Mutation in Estrogen Receptor-alpha: A Novel Mechanism for Acquired Endocrine Resistance in Breast Cancer. Cancer Res 2013;73:6856-64.
- Robinson DR, Wu YM, Vats P, Su F, Lonigro RJ, Cao X, et al. Activating ESR1 mutations in hormone-resistant metastatic breast cancer. Nat Genet 2013.
- Toy W, Shen Y, Won H, Green B, Sakr RA, Will M, et al. ESR1 ligand-binding domain mutations in hormone-resistant breast cancer. Nat Genet 2013.
- Baselga J, Campone M, Piccart M, Burris HA, 3rd, Rugo HS, Sahmoud T, et al. Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer. N Engl J Med 2012;366:520-9.
- Wolff AC, Lazar AA, Bondarenko I, Garin AM, Brincat S, Chow L, et al. Randomized phase III placebo-controlled trial of letrozole plus oral temsirolimus as first-line endocrine therapy in postmenopausal women with locally advanced or metastatic breast cancer. J Clin Oncol 2013;31:195-202.
- Baselga J. Targeting the phosphoinositide-3 (PI3) kinase pathway in breast cancer. Oncologist 2011;16 Suppl 1:12-9.
- The-Cancer-Genome-Atlas-Network. Comprehensive molecular portraits of human breast tumours. Nature 2012;490:61-70.
- Austreid E, Lonning PE, Eikesdal HP. The emergence of targeted drugs in breast cancer to prevent resistance to endocrine treatment and chemotherapy. Expert Opin Pharmacother 2014;15.
- Slamon DJ, Leyland-Jones B, Shak S, Fuchs H, Paton V, Bajamonde A, et al. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2. N Engl J Med 2001;344:783-92.
- Grunwald V, DeGraffenried L, Russel D, Friedrichs WE, Ray RB, Hidalgo M. Inhibitors of mTOR reverse doxorubicin resistance conferred by PTEN status in prostate cancer cells. Cancer Res 2002;62:6141-5.
- Clark AS, West K, Streicher S, Dennis PA. Constitutive and inducible Akt activity promotes resistance to chemotherapy, trastuzumab, or tamoxifen in breast cancer cells. Mol Cancer Ther 2002;1:707-17.
- Wallin JJ, Guan J, Prior WW, Edgar KA, Kassees R, Sampath D, et al. Nuclear phospho-Akt increase predicts synergy of PI3K inhibition and doxorubicin in breast and ovarian cancer. Sci Transl Med 2010;2:48ra66.




